Förutsäga formler av föreningar med polyatomiska joner
 Share
Share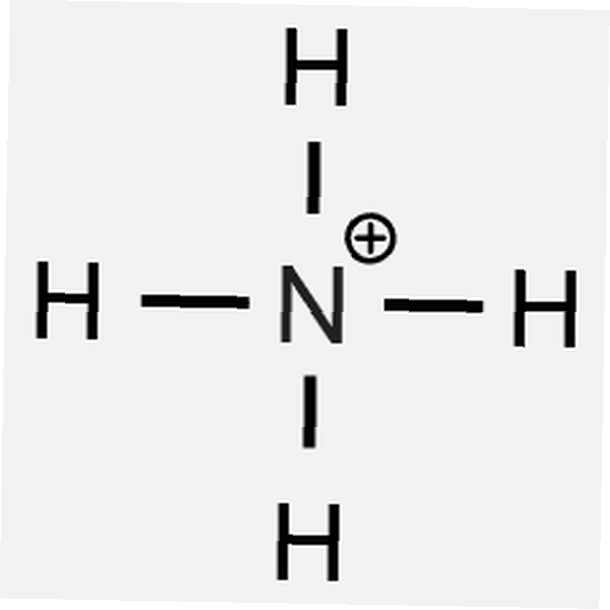
Polyatomiska joner är joner som består av mer än ett atomelement. Detta exempelproblem visar hur man kan förutsäga molekylformlerna för flera föreningar som involverar polyatomiska joner.
Polyatomiskt jonproblem
Förutse formlerna för dessa föreningar, som innehåller polyatomiska joner:
- bariumhydroxid
- ammoniumfosfat
- kaliumsulfat
Lösning
Formlerna för föreningar som innehåller polyatomiska joner finns på ungefär samma sätt som formler för monoatomiska joner. Se till att du är bekant med de vanligaste polyatomiska jonerna. Här är en lista över polyatomiska joner som hjälper dig. Titta på platserna för elementen i det periodiska systemet. Atomer i samma kolumn som varandra (grupp) tenderar att uppvisa liknande egenskaper, inklusive antalet elektroner elementen skulle behöva vinna eller förlora för att likna den närmaste ädelgasatomen. För att bestämma vanliga joniska föreningar som bildas av element, tänk på följande:
- Grupp I-joner (alkalimetaller) har +1-laddningar.
- Grupp 2-joner (jordalkalimetaller) har +2-laddningar.
- Grupp 6-joner (icke-metaller) har -2 avgifter.
- Grupp 7-joner (halider) har -1 avgifter.
- Det finns inget enkelt sätt att förutsäga laddningarna för övergångsmetallerna. Titta på en tabell som visar avgifter (valenser) för möjliga värden. För introduktions- och allmänkemikurser används oftast +1, +2 och +3-avgifterna.
När du skriver formeln för en jonisk förening, kom ihåg att den positiva jonen alltid listas först. Om det finns två eller flera polyatomiska joner i en formel, stäng den polyatomiska jonen i parentes.
Skriv ner den information du har om laddningarna för komponentjonerna och balansera dem för att svara på problemet.
- Barium har en +2-laddning och hydroxid har därför -1-laddning
1 Ba2+ jon krävs för att balansera 2 OH- joner - Ammonium har en +1-laddning och fosfat har därför en -3-laddning
3 NH4+ joner krävs för att balansera 1 PO43- Jon - Kalium har en +1-laddning och sulfat har därför -2-laddning
2 K+ joner krävs för att balansera 1 SO42- Jon
Svar
- Ba (OH)2
- (NH4)3PO4
- K2SÅ4
De avgifter som anges ovan för atomer inom grupper är de vanliga avgifterna, men du bör vara medveten om att elementen ibland tar olika avgifter. Se tabellen över elementens valenser för en lista över de laddningar som elementen har varit kända för att anta. Till exempel antar kol ofta antingen ett +4- eller -4-oxidationstillstånd, medan koppar vanligtvis har som +1 eller +2-oxidationstillstånd.
